Resumo sobre Termoquímica - Química

Entalpia (H)
- Conteúdo energético de uma determinada substância
- Reação endotérmica: absorção de energia
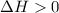
- Reação exotérmica: liberação de energia
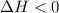
Quanto maior for, mais fortes são as ligações entre as moléculas
Conceito
Estuda as trocas de calor/energia em reações químicas
- Envolve variação de temperatura
- Calor é transformado e conservado
- Rearranjo de átomos e conservação da massa
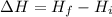
Calor de Reação
É o calor liberado ou absorvido na reação química
Extensivo (depende da quantidade)
Calor de Combustão
É o calor liberado na combustão completa de 1 mol de substância (EP)
Completa: 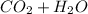
Incompleta: 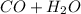
Lei de Hess
Como o 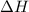 das etapas é possível chegar ao
das etapas é possível chegar ao 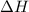 da equação global
da equação global
Representações Termodinâmicas
Exemplo:
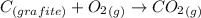
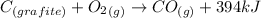
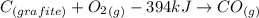
Observações
Na equação, deve-se evidenciar o estado físico, o 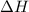 observar o estado padrão, pois o que é considerado é o Estado Padrão (EP) da substância.
observar o estado padrão, pois o que é considerado é o Estado Padrão (EP) da substância.
A forma mais abundante na natureza (a 25°C e 1 atm)
Calor de Formação
É o calor envolvido na formação de 1 mol de substância, a partir de substâncias simples, considerando o Estado Padrão 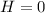
Exemplo:
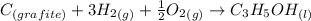
Estude agora:



