Resumo sobre Massa Atômica, Massa Molecular, Mol e Massa Molar - Química

Massa Atômica e Molecular
Átomo de 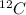
Padrão: 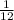 do
do 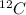
Equivalente a 1 u
Unidade de massa atômica (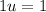 )
)
Massa Atômica (ma)
- Massa de um átomo;
- Indica quantas vezes o átomo é mais pesado que o padrão.
Exemplo: Mg: 24 u, pesa 24u
24x mais pesado que o carbono-12
Massa do Elemento - Isótopos
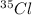 : 35 u, abundância na natureza (x%)
: 35 u, abundância na natureza (x%)
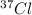 : 37 u, abundância na natureza (y%)
: 37 u, abundância na natureza (y%)
Média ponderada do cloro
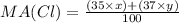
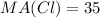
Na tabela periódica, as massas atômicas dos elementos químicos são as médias ponderadas de seus isótopos encontrados.
Massa Molecular (mm)
- Massa de uma molécula.
Exemplo: 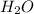 : H = 1 u x 2, O = 16 u x 1
: H = 1 u x 2, O = 16 u x 1
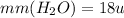
Moletagem: @studyanannaflavia
- Quantidade de matéria que contém.
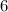 - constante de Avogadro
- constante de Avogadro
1 mol = 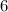 ou
ou 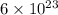
Massa Molar (M)
Unidade: g/mol
Exemplo: H O: 1 mol de moléculas =
O: 1 mol de moléculas = 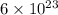 moléculas
moléculas
2H = 2 x 1 = 2 átomos, 3 mol de átomos
O = 16 átomos, 3 mol de átomos
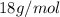
1) Verificar quantas moléculas do composto
2) Verificar quantos átomos presentes no composto
3) Número de átomos x constante de Avogadro
4) Soma das MA de todos os átomos presentes
Número de mols (n)
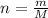
unidade: mol
m = massa
M = massa molar
Exercício
Quantos átomos há em 3 mols de moléculas de gás carbônico?
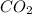
1 mol de moléculas
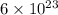 moléculas
moléculas
3 mols de átomos
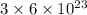 átomos
átomos
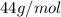
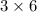 átomos = 1 mol de moléculas
átomos = 1 mol de moléculas
Logo, 3 mols de moléculas
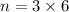
 átomos
átomos
Exercício por: Marcação: @studyanannaflavia
Estude agora:



